PRACTICA # 15
PRESENTADO POR : GRUPO: # 2
INDICADORES DE PH
OBJETIVO GENERAL:
* Elaborar un indicador de pH a partir del repollo morado
OBJETIVO ESPECIFICO:
* Determinar cada uno de los grados de las diferentes soluciones
MATERIALES
- Hojas de repolllo morado
- Jugo de limon
- Papel filtro
- Montaje para filtracion simple
- 1 Mortero con pistilo
- 1 Vaso de precipitados de 100ml
- 5 Tubos de ensayo
- 1 Gradilla
- 1 Gotero
- 1 Pipeta graduada de 1 ml
REACTIVOS
- Amoniaco NH3
- sln de Acido Clorhidrico HCl
- sln deHidroxido de sodio, NaOH
- Metano CH3OH
- Vinagre diluido CH3COOh
Un indicador es sustancia natural o sintética que cambia de color en respuesta a la naturaleza de su medio químico. Los indicadores se utilizan para obtener información sobre el grado de acidez o pH de una sustancia, o sobre el estado de una reacción química en una disolución que se está valorando o analizando. Uno de los indicadores más antiguos es el tornasol (el papel tornasol rojo se vuelve azul cuando se humedece con una solución básica; el papel tornasol azul se vuelve rojo al humedecerse con una solución ácida), un tinte vegetal que adquiere color rojo en las disoluciones ácidas y azul en las básicas. Otros indicadores son la alizarina, el rojo de metilo y la fenolftaleína; cada uno de ellos es útil en un intervalo particular de acidez o para un cierto tipo de reacción química. Los indicadores pueden ser naturales o artificiales.
En la tabla se muestran algunos indicadores ácido-base, o de pH, con sus intervalos de viraje (intervalos de pH en los que cambian de color) y sus distintos colores según se encuentren en medio ácido o básico:
Nombre de la
Sustancia
|
Intervalo
de pH
|
Color del
Ácido
|
Color de
La Base
|
| Azul de bromofenol | 3,0 - 4,6 | Amarillo | Púrpura |
| Anaranjado de metilo | 3.1-4.4 | Rojo | Amarillo |
| Rojo de metilo | 4.2-6.2 | Rojo | Amarillo |
| Azul de bromotimol | 6.0-7.6 | Amarillo | Azul |
| Tornasol | 5.8-8.0 | Rojo | Azul |
| Fenolftaleína | 8.0-9.8 | Incoloro | Rojo – Violeta |
| Amarillo de alizarina | 10.1-12.0 | Amarillo | Violeta |
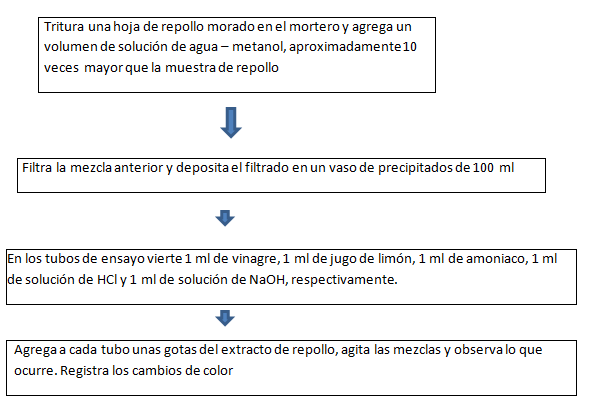
DIAGRAMA DE FLUJO
DISCUSIÓN DE RESULTADOS
1 ¿Cuales de las sustancias utilizadas son ácidas?
- Limón
- Vinagre
- HCl
2 ¿ Cuales de las sustancias utilizadas son básicas?
- NaOH
3 ¿ Que coloraciones toma el repollo en presencia de ácidos y bases?
- Lila
- Blanco
- Azul claro
- Rosado claro
- Rosada fuerte
4 ¿ Porque la solución de repollo morado se puede considerar un indicador ácido - base?
°Repollo morado: es una planta de la familia del repollo (y ambas de las coles). Es una variedad de col en la que las hojas poseen un color violáceo característico. su color se debe a la presencia de un pigmento llamado antocianina. La fuerza de este color puede depender en gran medida de la acidez (pH) del suelo, las hojas crecen más rojas en suelos de carácter ácido mientras que en los alcalinos son más azules.
5 ¿ Que otros vegetales se pueden utilizar para elaborar indicadores de pH?
Las charconas y auronas viran de amarillo a rojo ; las flaconas e isoflavonas varían de diversos tonos de rojo. Los flavoles de cafe a anaranjado . Anticioninas - azul
Los flavonoides pigmentos vegetales que toman color amarillo en presencia de vapores de amoniaco ( Pétalos blanco - flores)
RESULTADOS
Tubo 1 : ( HCl)
Al agregarle las 10 gotas de metanol se separo un momento del NaOH y con la sustancia de repollo morado se obtuvo un color lila .
Tubo 2: (Agua oxigenada)
Al agregarle el zumo de repollo no se nota cambio y con las gotas de etanol tampoco
Tubo 3: ( NaOH)
Con el zumo dio un color azul claro y con el metanol no se noto ningún cambio
Tubo 4: (Vinagre)
Con las gotas de metanol tomo un color rosado claro y con el zumo nada
Tubo 5: ( Limón)
Con el zumo de repollo dio un color lila mas fuerte.
CONCLUSIONES
- Aprendimos a elaborar un indicador de pH a partir del repollo morado en el cual determinamos algunos cambios con diferentes químicos.
- Se utilizan como indicador de las sustancias químicas que cambian su color al cambiar el pH de la solución .










No hay comentarios:
Publicar un comentario